劉長梅團隊揭示組蛋白修飾在腦疾病與神經再生中的關鍵功能與調控機製
神經係統是人體結構和功能最複雜的係統,作為人體的指揮中心,負責調控運動、學習、記憶、感知和情緒等多種功能。神經元是神經係統中最主要的細胞類型,承擔著信號傳導的核心任務。神經元在成熟後並非一成不變,它們對損傷和疾病極為敏感,如以神經元進行性丟失為特征的神經退行性疾病,這些疾病的核心症狀是神經網絡結構和功能的崩潰,最終導致記憶、認知、行為和運動功能的損害,神經功能的恢複依賴於神經再生和神經元功能的重建。
組蛋白修飾作為表觀遺傳調控的核心機製之一,近年來成為研究熱點。組蛋白修飾通過化學修飾(如甲基化、乙酰化、磷酸化等)動態調控染色質結構和基因轉錄活性,從而影響神經幹細胞的命運決定、神經元的功能成熟以及神經再生過程。其中,組蛋白H3第27位賴氨酸的三甲基化(H3K27me3)在大腦發育和神經再生中尤為重要。H3K27me3通常與基因沉默相關,通過調控關鍵基因的表達,精細調控神經係統的發育和功能。必威精装版app西汉姆联 劉長梅研究組及其合作者圍繞組蛋白修飾,開展了一係列的研究工作,揭示其在神經發育與神經再生中重要的功能以及調節機製。最新研究成果發表在Adv Sci (Weinh)。
1. 組蛋白修飾在原位神經再生中的調控機製
劉長梅研究組圍繞 H3K27me3 展開深入研究,從 “組蛋白修飾” 層麵逐步深入到 “基因功能” 層麵,揭示了其在原位神經再生及神經發育調控過程中的功能與相應機製。通過篩選,發現急性損傷的神經再生模型中H3K27me3升高,進而圍繞視神經節細胞的存活與再生,建立了多種相關的疾病模型,急性視神經損傷模型(RGCs存活和視神經再生)、NMDA模型(RGCs存活)和微球注射模型(青光眼高眼壓模型),在此基礎上,研究組與浙江大學周峰泉教授團隊揭示了H3K27甲基轉移酶EZH2通過調控H3K27me3修飾,激活軸突再生相關基因的表達,從而促進RGCs的存活和軸突再生(Journal of Clinical Investigation,2024),提示H3K27me3升高有利於神經再生。研究組與合作團隊通過兩種H3K27me3去甲基化酶 UTX/JMJD3的缺失,進一步探究了其在神經保護和軸突再生中的功能。結果顯示缺失 UTX 或 JMJD3 會導致周圍神經係統 (PNS) 中的軸突原位再生能力增強,而在中樞神經係統 (CNS)中,隻有UTX在RGCs 中缺失後會增強視神經再生的功能,但是UTX/JMJD3都具有調節 RGCs 存活的功能,機製不同。RNA-seq 分析顯示 UTX 缺失將 RGC 轉錄組學逆轉到發育樣狀態,Klf4 是周圍神經係統DRG神經元和視網膜RGCs中UTX-H3K27me3 信號轉導的直接下遊靶標。這些發現不僅揭示了UTX和JMJD3在神經再生中的不同作用及其潛在機製,而且還確定了UTX介導的組蛋白去甲基化信號轉導是支持CNS神經再生的新型表觀遺傳靶標(Advanced Science,2025)。
與此同時,劉長梅研究組與北京同仁醫院王寧利教授合作,揭示了H3K27me3下遊的一個靶標轉錄因子LHX2與組蛋白修飾協同作用,促進RGCs存活和軸突再生的機製。研究表明,LHX2通過激活再生相關基因的表達,為青光眼等神經退行性疾病的治療提供了新的策略(Cell Reports Medicine,2024)。這些研究提示,通過調控EZH2、UTX或LHX2的表達,可以將成體神經元的轉錄組圖譜逆轉至更具神經生長能力的年輕狀態,從而促進神經再生。
2. 組蛋白修飾在神經元發育中的調控作用
組蛋白修飾不僅在神經再生中發揮重要作用,還深刻影響神經發育過程。劉長梅課題組研究發現,組蛋白甲基轉移酶PRC2(多梳抑製複合物2)的核心亞基EED在胚胎期皮層發育和海馬齒狀回發育中具有重要功能。EED通過催化H3K27me3修飾,調控Gli3、Gli1、Cdkn2a、Sox11等關鍵基因的表達,從而影響神經幹/祖細胞(NSPCs)的增殖和分化(Stem Cell Reports,2019;Stem Cell Reports,2022)。H3K27me3修飾的異常導致神經幹細胞分化受阻,進而影響皮質神經發生和海馬齒狀回的正常發育。
此外,研究組還首次揭示了染色質重塑SWI/SNF複合體組分ARID1A通過介導特定位點組蛋白修飾,調控海馬區神經幹/祖細胞向神經元譜係轉變的功能(Cell Death and Differentiation,2023)。ARID1A缺失會導致小鼠海馬突觸傳遞和樹突形態缺陷引起的認知障礙,以及人類興奮性神經元的樹突分支和電生理活動異常。值得注意的是,補充表觀遺傳代謝物乙酸鹽可以改善ARID1A缺失引起的形態學和電生理學缺陷,提示乙酸鹽可能成為Coffin-Siris綜合征(CSS)的潛在治療幹預措施(EMBO Molecular Medicine,2022)。
小腦在運動協調、平衡控製以及感覺運動學習等方麵發揮著核心作用。研究發現,組蛋白H3K27me3修飾異常會導致小腦發育缺陷,進而引發一係列運動和認知障礙。EED作為PRC2的核心亞基,通過催化H3K27me3修飾,與非編碼RNA H19形成負反饋調節環路,精細調控小腦顆粒細胞祖細胞的增殖、分化和凋亡過程(Advanced Science,2025)。這一發現為理解小腦發育缺陷及相關疾病的發病機製提供了重要依據。
3.組蛋白修飾研究的科學意義與應用前景
上述關於組蛋白修飾的一係列研究成果,具有重要的科學意義和應用價值。在基礎研究領域,這些成果極大地拓展了我們對大腦發育和神經發育以及神經再生障礙疾病發病機製的認知,讓我們對基因表達調控的複雜性和精細性有了更為深刻的理解。在臨床應用方麵,這些發現為開發新型診斷和治療方法提供了潛在的靶點。例如,針對特定組蛋白修飾異常設計的幹預措施,有望成為治療自閉症、小腦發育不全等神經發育疾病的創新幹預手段。
綜上所述,隨著對組蛋白修飾研究的持續深入,我們有理由相信,未來能夠進一步揭開其在大腦發育和疾病中的神秘麵紗,為改善人類健康帶來更多的希望。該係列研究得到了國家重點研發計劃項目、中國科學院先導項目、中國科學院青年創新促進會、國家自然基金項目、必威精装版app西汉姆联 自主部署項目以及器官再生與智造國家重點實驗室開放項目等基金的資助。

(必威精装版app西汉姆联 劉長梅團隊,北京基因組研究所楊運桂團隊,必威精装版app西汉姆联 /北京幹細胞與再生醫學研究院滕兆乾團隊和南京醫科大學李榮鳳團隊共同完成)

(J Clin Invest,2024;Cell Rep Med,2024;Advanced Science,2025)

(EMBO Mol Med,2022;Cell Death Differ,2023)

(Advanced Science,2025)

全球約三分之一陸地生物多樣性熱點區域以及60%的陸棲脊椎動物分布在跨境地帶,這些區域同時也麵臨生物入侵、氣候變化、生境幹擾等諸多全球變化挑戰。自然保護地是維係本土物種原生性和抵禦外來物種入侵的重要載體...
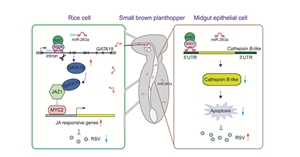
蟲媒植物病毒的感染涉及病毒、媒介昆蟲和植物寄主之間的複雜互動。大約80%的植物病毒依賴昆蟲傳播,通常在植物體內而非昆蟲媒介中引發嚴重症狀。
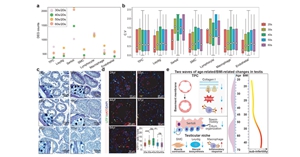
為了研究衰老對男性生殖的影響,中國科學院院必威在线网址 /北京幹細胞與再生醫學研究院郭靖濤研究組此前係統研究並揭示了年輕(20多歲)和年老(60歲以上)男性睾丸的分子和轉錄差異,並發現衰老和肥胖疊加會顯著加...

